- Услуги
- Цена и срок
- О компании
- Контакты
- Способы оплаты
- Гарантии
- Отзывы
- Вакансии
- Блог
- Справочник
- Заказать консультацию
Заказать консультацию
Теория Дебая–Хюккеля
Коэффициенты активности ионов зависят от многих факторов, но основным является электростатическое взаимодействие ионов, на основании чего был получен предельный закон Дебая–Хюккеля.
Интересно
Как изображено на рис. 1.12, ион в растворе окружен большим количеством противоположно заряженных ионов (противоионов), чем одноименно заряженных, что приводит к некоторому экранированию заряда центрального иона.
Энтропия имеет самое высокое значение, если все ионы распределены в растворе хаотично, но энергия электростатического притяжения между противоположно заряженными ионами пытается выстроить ионы в правильно построенную решетку.
Электростатическое притяжение сильнее, если ионы находятся ближе друг к другу и, следовательно, чем выше концентрация ионов, тем сильнее экранирование заряда центрального иона (рис. 1.12).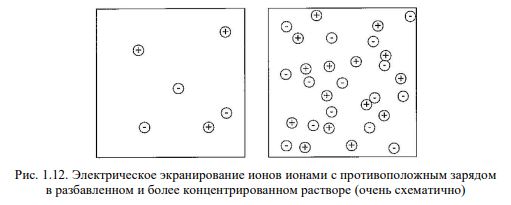
Поскольку в этом принимают участие все ионы, находящиеся в растворе, вводится понятие общей ионной силы раствора, определяемое по формуле (1.49):

Так, 0,01 М раствор СаСl² имеет ионную силу М. Большинство пищевых продуктов, содержащих большое количество воды, имеет ионную силу от 1 до 100 ммоль • л-1.
Согласно теории, влияние оказывает и размер иона; взяв среднее значение размера иона, средне – ионный коэффициент активности соли в разбавленном растворе можно приблизительно рассчитать по формуле (1.50а):

Таким образом, чем выше ионная сила раствора, больше заряды ионов и меньше диэлектрическая постоянная, тем меньше средне – ионный коэффициент активности. Для воды при 20 °С величина ε= 80, и уравнение (1.50а) принимает вид (1.50б):
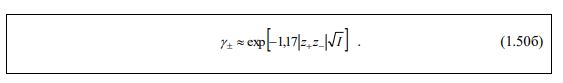
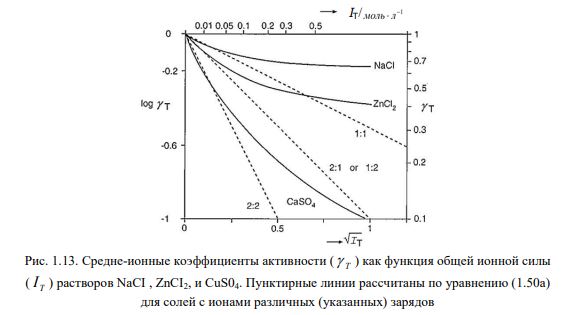
Большое влияние оказывает заряд ионов; сравнивая, к примеру, 0,01 М раствор NaCI с 0,01 М раствором CaS04, получим коэффициенты активности 0,89 и 0,31 соответственно. На рис. 1.13 представлены средне – ионные коэффициенты активности нескольких растворов соли, а для сравнения даны их рассчитанные значения.
Следует заметить, что уравнение (1.50а) не учитывает природу ионов. Практически для большинства неорганических ионов различия действительно невелики, за исключением кислот, для которых величина средне – ионного коэффициента активности выше, чем следует из уравнения (1.50а).
Статьи по теме
- Силы внутреннего трения жидкости. Уравнение Ньютона
- Идеальные модели деформирующихся систем
- Основные понятия реологии
- Учение о процессах деформации систем
- Теория абсолютных скоростей реакции
- Температурная зависимость скорости реакции
- Растворы электролитов при диссоциации
- Самоассоциация и электрическое экранирование
- Адсорбция как отклонение
Полезные статьи









Узнайте цену услуг:
Узнай цену консультации
"Да забей ты на эти
дипломы и экзамены!”
(дворник Кузьмич)

